Neatkarīgā komiteja, kas konsultē FDA, šo jautājumu izskatīs sanāksmē ceturtdien.
Dati, kas ASV iegūti no 38 000 izmēģinājuma dalībnieku, "liecina par labvēlīgu drošības profilu bez specifiskām bažām par drošību, kas liegtu izsniegt atļauju ārkārtas pielietojumam", teikts FDA dokumentā.
Vakcīnas efektivitāte aizsardzībā pret Covid-19 ir 95%, tā darbojusies vienādi labi visās vecuma grupās, pie abu dzimumu pārstāvjiem, visās rasu grupās, kā arī pie cilvēkiem ar pamatslimībām, kas pakļauti lielākam riskam.
Ir vajadzīga papildu izpēte, lai gūtu apstiprinājumu liecībām, ka vakcīna aizsargā pret smagākajiem Covid-19 gadījumiem, ka tā nodrošina aizsardzību arī tad, ja ir saņemta pirmā no divām devām, kā arī tā ir iedarbīga arī pie cilvēkiem, kas bijuši inficēti iepriekš.
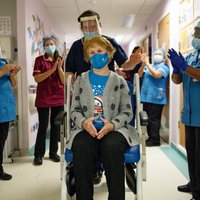
Jau ziņots, ka Lielbritānijas Nacionālais veselības dienests 8. decembrī sācis programmu iedzīvotāju vakcinēšanai pret Covid-19.
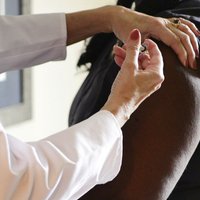
Aptuveni 70 slimnīcās visā Lielbritānijā cilvēkiem, kas vecāki par 80 gadiem, un veselības aprūpes darbiniekiem tiks injicēta ASV farmācijas giganta "Pfizer" un Vācijas kompānijas "BioNTech" izstrādātā vakcīna pret jauno koronavīrusu.
Lielbritānija ir pirmā valsts pasaulē, kas izmantos šo vakcīnu, ko Lielbritānijas zāļu aģentūra apstiprināja pagājušajā nedēļā.