
Vienkārši organismi ar milzīgu funkcionalitāti
Baktērijas ir salīdzinoši vienkārši organismi, to šūnas nesatur daudzas augu vai dzīvnieku šūnās raksturīgās struktūras, tostarp, kodolu, mitohondrijus, hloroplastus. Taču arī baktēriju šūnās reizēm veidojas atsevišķi nodalījumi, kuri noteiktos apstākļos būtiski atvieglo svarīgu ķīmisko reakciju norisi. Tie ir mikronodalījumi (angliski – microcompartment). Tie ir proteīnu apvalkā ieslēgtas jeb iekapsulētas enzīmu grupas, kas kopīgi realizē kādu organismam svarīgu funkciju, piemēram, veic oglekļa fiksāciju vai noteiktu vielu šķelšanu. Atkarībā no iekapsulētajiem enzīmiem, pašreiz ir aprakstīti ap 30 dažādi baktēriju mikronodalījumu veidi, bet tikai dažiem no tiem ir raksturota gan uzbūve, gan 3D struktūra.
Baktērijā Klebsiella pneumoniae sastopamie holīna liāzes mikronodalījumi bija galvenais pētījuma objekts. Tās ir nelielas proteīnu kapsulas, kuru diametrs ir 25-50 nm. Līdzīgi kā futbolbumbu veido regulāri atkārtoti piecstūru un sešstūru segmenti, arī mikronodalījuma "čaulu" veido vairākkārt atkārtoti proteīnu pentamēri un heksamēri. Čaulas iekšpusē savukārt atrodams galvenais enzīms – holīna liāze – un palīgenzīmi, tostarp, alkohola dehidrogenāze, acetaldehīda dehidrognāze un citi.
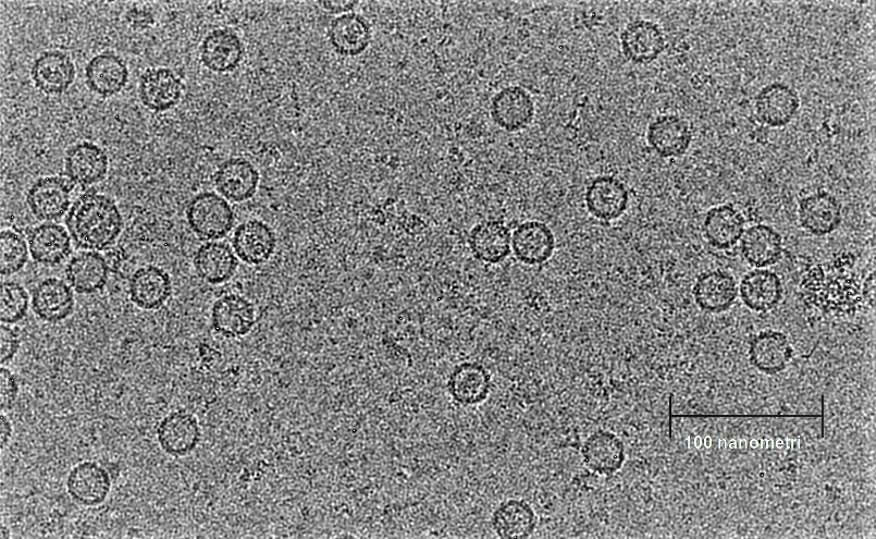
Izrādījās, ka šos mikronodalījumus iespējams "ražot" citā, molekulārajā bioloģijā ierastā, baktērijā –zarnu nūjiņā. Taču ne vienmēr notika enzīmu "pašsavākšanās" gaidītajā mikronodalījumā. Izrādījās, ka enzīmu pašsavākšanās notiek tad, ja ir klātesošs "galvenais" mikronodalījuma enzīms – holīna liāze. Ar krioelektronmikroskopijas un caurstarojošās elektronmikroskopijas palīdzību izdevās noskaidrot precīzu mikronodalījumu izmērus un ārējo uzbūvi. Uzsākot pētījumu 2018. gada sākumā, pasaulē bija zināma tikai viena tipa baktēriju mikronodalījumu struktūra, turklāt nebija zināmi principi, kā enzīmi pašsavācas mikronodalījumos.
Būtisks solis specifisku bioķīmisko sistēmu radīšanā
LU un BMC pētnieku komanda sniegusi vērtīgu ieguvumu fundamentālajā zinātnē. "Nature Communications" atvērtās pieejas publikācijā pirmoreiz ir parādīts, ka centrālais enzīms – holīna liāze – ir faktors, kas nodrošina pārējo trīs enzīmu iepakošanu.
"Līdz šim iespējamība, ka tieši tā notiek enzīmu iepakošana mikronodalījumos, bija aprakstīta teorētiski, taču nebija praktiski parādīta, ka tik tiešām iepakošanas jeb enkapsulācijas procesam raksturīga noteikta hierarhija. Proti, katram enzīmam ir sava, neatdalāma loma veiksmīgā iepakošanas procesā. Tāpat arī mums pirmajiem izdevās novērot konkrētajam mikronodalījuma veidam unikālu, līdz šim neraksturotu struktūru," gandarīts ir BMC zinātniskais asistents, LU Bioloģijas fakultātes (BF) doktora grāda pretendents Gints Kalniņš, kuram pētījums ir daļa no promocijas darba struktūrbioloģijas jomā.
Enkapsulējot jeb iepakojot konkrētus enzīmus mikronodalījumos, varētu iegūtu stabilas bioķīmiskās sistēmas, kas realizētu tikai produkta ieguvei nepieciešamās reakcijas. Lai to paveiktu, jāzina, pēc kādiem principiem norit mikronodalījuma veidošanās un enzīmu iekļaušanās tajos. Paveiktais pētījums ir būtisks solis, lai virzītos uz šo mērķi, un mikronodalījumos patiešām varētu ievietot mums interesējošus enzīmus," skaidro Liepiņš.
Publikācijas autoru lokā ir arī LU BF maģistrante, BMC laborante un trīskārtējā LU fonda stipendiāte Eva Emīlija Česle, BMC grupas vadītājs, vadošais pētnieks Kaspars Tārs, pētnieks Juris Jansons, kā arī sadarbības partneris no Masarika Universitātes Brno, Čehijas Republikā, Anatolijs Filimoņenko.

Īstenojot šo "Mikrotīkls" atbalstīto LU un BMC sadarbības projektu, pētnieku komanda ir atklājusi jaunas iespējas Latvijas zinātniekiem iesaistīties starptautiski aktuālā un no pielietojuma viedokļa daudzsološā pētījumu jomā. Turklāt komandai ir izdevies pierādīt savu zinātnisko kompetenci šajā jomā, ziņojot par iegūtajiem rezultātiem augstas raudzes žurnālā, kura impakta faktors ir 11,8.
Pētījums ir īstenots projekta "Baktēriju mikrokompartmenti kā sintētiski nanoreaktori" ietvaros. Tā rezultātus prezentēs 26. martā, piedaloties Mičiganas Štata universitātes (ASV) profesorei Šerilai Kerfeldai, kas ir viena no vadošajām baktēriju mikronodalījumu pētniecēm un viena no šīs jomas pamatlicējām. Projekta vadītājs ir LU Mikrobioloģijas un biotehnoloģiju institūta vadošais pētnieks, bioloģijas zinātņu doktors Jānis Liepiņš. Ar LU fonda administratīvu atbalstu projekta veiksmīgu norisi nodrošināja mecenāta SIA "Mikrotīkls" ziedojums.



